摘要:
莘县中心医院山东莘县 252423摘要:目的:分析化疗联合免疫治疗与单纯化疗治疗中晚期非小细胞肺癌的效果。方法:实验时间确定在2021年1月-2023年1月之间,抽取该阶段中晚期非小细胞肺癌患者80例,以随机抽签法分组,组别设为对照组、试验组,每组患者各40例,对照组使用单纯化疗治疗,试验组使用化疗联合莘县中心医院 山东莘县 252423
摘要:目的:分析化疗联合免疫治疗与单纯化疗治疗中晚期非小细胞肺癌的效果。方法:实验时间确定在2021年1月-2023年1月之间,抽取该阶段中晚期非小细胞肺癌患者80例,以随机抽签法分组,组别设为对照组、试验组,每组患者各40例,对照组使用单纯化疗治疗,试验组使用化疗联合免疫治疗,对比两组血清肿瘤标志物、癌胚抗原、免疫功能以及不良反应发生率。结果:治疗前两组血清肿瘤标志物指标对比无差异,P>0.05;治疗后试验组CYFRA211、CEA、NK、CA125指标均低于对照组,P<0.05。治疗前两组免疫功能指标对比无差异,P>0.05;治疗后试验组CD4、NK指标高于对照组,CD8指标低于对照组,P<0.05。试验组不良反应发生率35.00%较对照组65.00%显著降低,P<0.05。结论:晚期非小细胞肺癌在单纯化疗治疗的基础上加入免疫治疗可更好的控制肿瘤进展,提升机体免疫能力,同时降低化疗期间的不良反应,值得推广。
关键词:化疗治疗;免疫治疗;中晚期;非小细胞肺癌;效果
肺癌属于全球范围内发病率较高的恶性肿瘤类型,其中非小细胞肺癌占肺癌发生率的80%。因肺癌起病较为隐匿,临床主要以疼痛、气促、咯血为特征,因此发现时疾病多处于中晚期,失去最佳手术时机,因此通过化疗等措施进行治疗,以延长生存周期。目前对于中晚期非小细胞肺癌主要使用铂类药物,但是长期单一使用化疗方法导致患者对于药物的敏感性不足,影响疾病治疗效果,因此需要对治疗方法进行改进。过继免疫治疗属于恶性肿瘤治疗的一个重要的辅助方法,可向靶向细胞回输免疫活性细胞,对于机体的免疫系统结构和功能损伤较小,但是可直接杀死肿瘤细胞,抗肿瘤活性高,并且不良反应少,成为恶性肿瘤治疗的重要组成部分[1]。本文对化疗联合免疫治疗与单纯化疗治疗中晚期非小细胞肺癌的效果进行对比分析,研究如下:
1资料与方法
1.1 一般资料
实验时间确定在2021年1月-2023年1月之间,抽取该阶段中晚期非小细胞肺癌患者80例,以随机抽签法分组,组别设为对照组、试验组,每组患者各40例。对照组男25例,女15例,年龄:42-78岁,中位年龄:(60.15±3.47)岁,腺癌23例、鳞癌17例。试验组男26例,女14例,年龄:42-77岁,中位年龄:(59.34±3.65)岁,腺癌22例、鳞癌18例。
纳入指标:①按照新编常见恶性肿瘤诊治规范对非小细胞肺癌的诊断标准,预计生存期在3个月以上[2];②存在咳嗽、痰血、胸痛症状[3];③影像学检测确定肺部肿块,存在疾病指征[4];④病理学诊断后确诊。⑤实验方案获批,患者签署实验同意书。
排除标准:①合并肝肾功能障碍;②合并精神疾病[2];③合并心脑血管疾病;④无完整就诊资料;⑤中途退出实验或死亡。
1.2方法
对照组-单纯化疗治疗,腺癌患者均进行吉西他滨联合顺铂化疗:吉西他滨在第1d、8d给药静脉滴注,剂量为1000mg/m2,30min滴注完成。顺铂在第1d、2d、3d给药静脉滴注,剂量为25mg/m2,以21d为一个周期;鳞癌患者进行紫杉醇联合顺铂化疗,紫杉醇在第1d静脉滴注,将135mg/m2加入500ml生理盐水中,用药前30min给予20mg地塞米松静脉注射,防止过敏反应。顺铂剂量在第1d、2d、3d给药,剂量80mg/m2,加入500ml生理盐水中稀释,药物治疗21d为一个周期。
试验组-化疗联合免疫治疗,化疗方法同上,在化疗开始第1d即抽取静脉血,进行细胞制备,将抽取血液样本以2000r/min速率离心,等待15min后使用磷酸盐缓释液冲洗离心后的血液样本,2次后对单核和细胞进行分离,后使用生理盐水进行清洗,将细胞浓度调整至1.5*107ml,使用无血清培养基进行重悬,将其接种于孔板中,等待8d获取成熟的DC-CIK细胞,在患者21d化疗结束后将DC-CIK细胞进行回输,在回输之前使用苯海拉明进行不良反应干预,在回输4次后继续进行下一疗程化疗。
1.3观察指标
①对比两组血清肿瘤标志物指标,使用酶联免疫吸附法对CYFRA211(细胞角蛋白19血清片段211)、CEA(癌胚抗原)、CA125(癌抗原125)指标进行分析。
②对比两组免疫功能,对T淋巴细胞CD4、CD8以及自然杀伤细胞NK进行分析。
③对比两组不良反应发生率,不良反应包括骨髓抑制、恶心呕吐和腹泻。
1.4统计学处理
本研究使用的统计学软件为SPSS23.0,计数资料表达方式为(x±s),进行统计学t值检验;计量资料表达方式为n(%),进行统计学卡方(X²)检验。两个项目经统计学分析最终可得到P值,检验差异显著的标准为P<0.05。
2结果
2.1对比两组血清肿瘤标志物指标
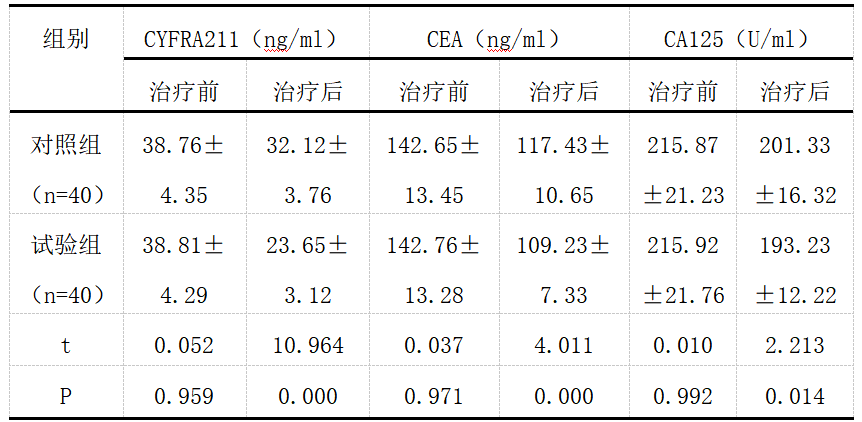
治疗前两组血清肿瘤标志物指标对比无差异,P>0.05;治疗后试验组CYFRA211、CEA、NK、CA125指标均低于对照组,P<0.05,详见表1。
表1对比两组血清肿瘤标志物指标(x±s)
2.3对比两组血清肿瘤标志物指标
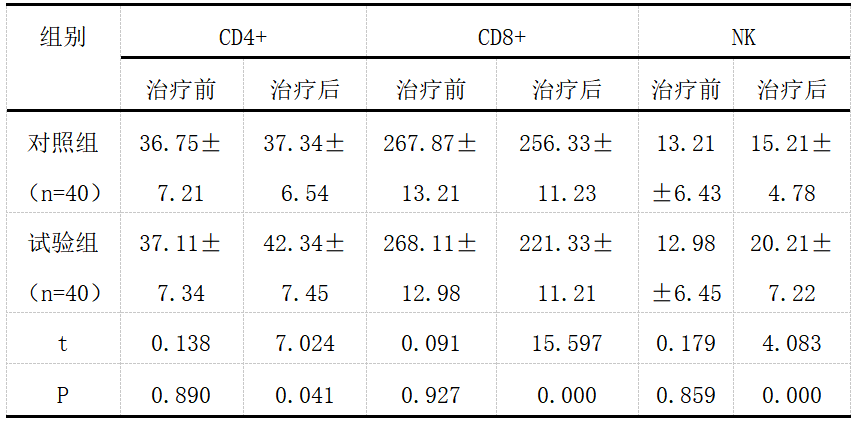
治疗前两组免疫功能指标对比无差异,P>0.05;治疗后试验组CD4、NK指标高于对照组,CD8指标低于对照组,P<0.05。详见表2。
表2对比两组血清肿瘤标志物指标(x±s,%)
2.3对比两组不良反应发生率
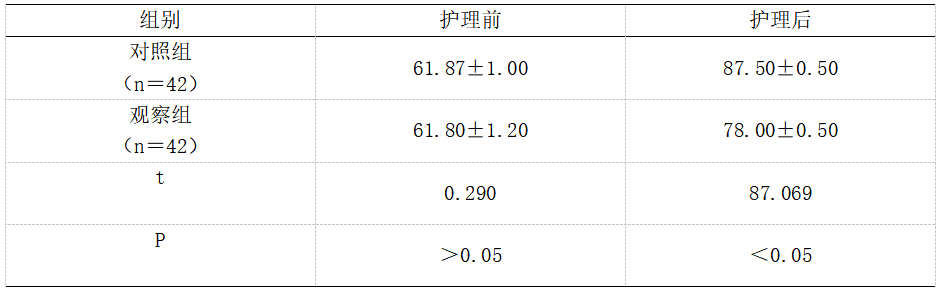
试验组不良反应发生率35.00%较对照组65.00%显著降低,P<0.05,详见表3。
表3对比两组不良反应发生率[n(%)]
3讨论
非小细胞肺癌导致的死亡位于我国恶性肿瘤死亡的首位,其中非小细胞肺癌占据肺癌总发病率的80%[5],与小细胞肺癌对比,该类型肺癌生长分裂较慢,扩散转移相对较晚,但是起病隐匿,患者发现时多数处于中晚期,手术治疗受到较大的限制,5年以上生存率较低[6]。化疗属于该病治疗的重要方法,但是一些患者对于化疗药物不敏感,并且副作用较大,影响整体治疗效果。随着对肺癌研究的不断深入,发现肺癌患者常呈现免疫功能抑制的情况,并且出现免疫漂移改变,导致细胞的免疫功能下降,使TH1向TH2漂移,对机体内抗肿瘤治疗造成非常严重的干扰,导致化疗过程中耐药性增加,导致化疗失败[7]。免疫治疗作为肿瘤治疗的一个重要辅助方法,将体外分离外周血中的免疫细胞通过一系列细胞因子、炎性因子刺激后,使其增殖并产生大量特定的功能性免疫细胞,后回输到患者体内,实现疾病的治疗,对于肿瘤的抑制具有积极作用[8-9]。
数据显示:治疗后试验组CYFRA211、CEA、NK、CA125指标均低于对照组,免疫指标显著提升,同时不良反应发生率降低,分析原因:CIK细胞属于对肿瘤细胞杀伤力较大的细胞,可直接作用于肿瘤细胞中,在受到敏感靶细胞刺激后会释放出大量的细胞毒性胞浆颗粒[10],对靶细胞造成直接的杀伤力,对于肿瘤产生直接的抑制作用,同时还可调节机体免疫反应,间接杀伤肿瘤细胞[11-12];CIK细胞通过对机体免疫功能的调节,促使T细胞增殖,而T细胞是构成机体免疫放于的重要因素,辅助性T细胞CD4+和抑制性细胞CD8+相互位置以保持免疫平衡,非小细胞肺癌患者因肿瘤细胞的影响[13],机体内CD4+下降,或者CD8+升高,导致机体免疫功能缺陷,而CIK细胞通过对免疫系统进行调节,维持CD4+、CD8+平衡,刺激NK细胞生长,并增加杀伤肿瘤细胞活性的能力,提升肿瘤控制质量;免疫治疗过程中加入了对不良反应的控制性药物,苯海拉明对于呕吐等消化道不良反应方面作用突出,因此联合用药可对药物治疗的不良反应进行控制[14-15]。
综上可见,中晚期非小细胞肺癌在单纯化疗治疗的基础上加入免疫治疗可更好的控制肿瘤进展,提升机体免疫能力,同时降低化疗期间的不良反应,值得推广。
参考文献
[1]王韵涵,孙亚楠,李鹏,等. 18F-FDG PET/CT代谢参数与晚期非小细胞肺癌一线免疫治疗联合化疗预后的关系 [J]. 中华放射医学与防护杂志,2023,43(2):87-93.
[2]张雨珊,韩毅,车南颖,等. 新辅助免疫治疗联合化疗对局部晚期非小细胞肺癌疗效的初步研究[J]. 中国医刊,2022,57(9):1016-1020.
[3]刘建清,骆华春,沈志勇,等. PLR和NLR与Ⅲ期非小细胞肺癌临床特征及同步放化疗联合免疫治疗疗效及预后的相关性[J]. 实用癌症杂志,2022,37(5):763-768.
[4]孙凤环,杨洁,葛韬,等. 新辅助抗PD-1免疫治疗联合化疗后手术治疗ⅢA期非小细胞肺癌临床分析[J]. 中华胸心血管外科杂志,2021,37(9):516-520.
[5]吴琼. DC-CIK细胞免疫治疗联合化疗在中晚期非小细胞肺癌治疗中的应用效果分析[J]. 中国社区医师,2021,37(3):66-67.
[6]林先勇,胡翔,殷海涛. 免疫治疗联合放化疗治疗非小细胞肺癌的临床研究进展[J]. 国际肿瘤学杂志,2022,49(1):56-60.
[7]李浩洋,秦娜,俞孟军,等. PD-L1高表达晚期非小细胞肺癌患者单纯免疫治疗与免疫联合化疗疗效比较[J]. 中国肺癌杂志,2021,24(3):161-166.
[8]张红娟,于振东,张艳平,等. 免疫治疗联合化疗在中晚期非小细胞肺癌治疗中的效果评价[J]. 中国医药指南,2020,18(13):69-70.
[9]张伟萍,应海峰,贺茹依,等. 细胞生物免疫治疗联合化疗对非小细胞肺癌患者凋亡相关基因和免疫功能的影响[J]. 中国基层医药,2021,28(6):806-810.
[10]贺竞,龙翔宇,王颖,等. PD-1/PD-L1免疫治疗联合多西他赛化疗方案治疗晚期复治性NSCLC的疗效及安全性[J]. 西部医学,2022,34(2):289-292.
[11]袁应选,李桥涛,袁琳. 同步放化疗联合DC-CIK细胞免疫治疗对NSCLC患者的预后及其肿瘤标志物的影响[J]. 医学临床研究,2022,39(8):1202-1205.
[12]张佳慧,郭其森,张初峰,等. EGFR 20外显子插入突变晚期NSCLC化疗联合免疫治疗对比联合贝伐珠单抗临床分析[J]. 中华肿瘤防治杂志,2022,29(11):828-833.
[13]杨森,谢颂平,龙杏林,等. 术前免疫检查点抑制剂联合化疗治疗可切除Ⅲ期非小细胞肺癌的疗效及患者近期预后的影响因素分析[J]. 实用心脑肺血管病杂志,2022,30(10):26-32.
[14]赵景景,李玲,谭于飞,等. 单纯化疗与免疫联合化疗对非小细胞肺癌患者炎性因子及免疫细胞的影响[J]. 实用癌症杂志,2022,37(6):917-921.
[15]陆舜,余新民,胡艳萍,等. 替雷利珠单抗联合化疗一线治疗局部晚期或转移性非鳞状非小细胞肺癌的肿瘤缓解特征[J]. 中华肿瘤杂志,2023,45(4):358-367.