摘要:
哈尔滨二四二医院 黑龙江哈尔滨 150066摘要:目的:分析不同核酸提取方法和新型冠状病毒核酸检测试剂室间质评结果。方法:选取2019年至2020年检验中心发放的新冠病毒核酸检测的样本60例,采用两种常见的核酸提取技术(磁珠法、核酸释放剂法),采用2个厂家生产的两种核酸扩增技术(RT-PCR),60例实验室内的 NCV核酸进行实验哈尔滨二四二医院 黑龙江哈尔滨 150066
摘要:目的:分析不同核酸提取方法和新型冠状病毒核酸检测试剂室间质评结果。方法:选取2019年至2020年检验中心发放的新冠病毒核酸检测的样本60例,采用两种常见的核酸提取技术(磁珠法、核酸释放剂法),采用2个厂家生产的两种核酸扩增技术(RT-PCR),60例实验室内的 NCV核酸进行实验室内的质评样品,对60个实验室内的 NCV核酸进行实验室内的质评样品进行分析,对两种实验室内常见的 NCV核酸提取技术(磁珠法、核酸释放剂法)和2个厂商的RT-PCR核酸扩增技术(RT-PCR)对样品进行分析,并对其进行分析,对比分析各种试剂对 NCV核酸的影响。结果:研究显示,60个样品中有49个样品呈阳性,11个样品呈阴性。采用核酸磁珠提取方法+ A厂商的核酸检测试剂对ORF1ab、 N基因的检出率分别为100.00%、两个基因的同时检出率分别为100.00%;核酸释放剂法+ B厂家核酸检测试剂阳性质评样品ORF1ab的检出率是70.00%, N基因的检出率是90.00%,两个基因的检出率是70.00%,有效检出率是90.00%;核酸磁珠提取法+ B厂商的核酸检测试剂对ORF1ab、 N基因的检出率分别为100.00%、两个基因的检出率分别为100.00%。3个配比的检测方法都不能检测到阳性样品,阳性一致性达到100%。结论:各种方法和方法对样品的定性评价存在较大差异,而采用的方法和试剂对样品的定性评价存在较大差异,需要进一步改进。
关键词:不同核酸提取方法;新型冠状病毒;核酸检测试剂;室间质评
Abstract: Objective: To analyze the results of external quality assessment of different nucleic acid extraction methods and novel coronavirus nucleic acid detection reagents. Methods: We selected 60 samples of COVID-19 nucleic acid detection issued by the testing center from 2019 to 2020, used two common nucleic acid extraction technologies (magnetic bead method, nucleic acid releaser method), two nucleic acid amplification technologies (RT-PCR) produced by two manufacturers, 60 NCV nucleic acids in laboratories were used for quality assessment samples in laboratories, and NCV nucleic acids in 60 laboratories were analyzed for quality assessment samples in laboratories, Analyze the samples using two common NCV nucleic acid extraction techniques (magnetic bead method and nucleic acid release agent method) and two manufacturers' RT PCR nucleic acid amplification techniques (RT PCR), and compare and analyze the effects of various reagents on NCV nucleic acid. Result: The study showed that out of 60 samples, 49 samples were positive and 11 samples were negative. The detection rates of ORF1ab and N genes using nucleic acid magnetic bead extraction method and manufacturer A's nucleic acid detection reagent were 100.00%, and the simultaneous detection rates of the two genes were 100.00%, respectively; The detection rate of ORF1ab, N gene, and two genes in the positive quality evaluation sample of the nucleic acid release agent method and B manufacturer's nucleic acid testing reagent is 70.00%, 90.00%, and 90.00%, respectively. The effective detection rate is 90.00%; The detection rates of ORF1ab and N genes using nucleic acid magnetic bead extraction method and manufacturer B's nucleic acid testing reagent were 100.00% and 100.00% respectively. The three matching detection methods cannot detect positive samples, and the positive consistency reaches 100%. Conclusion: There are significant differences in the qualitative evaluation of samples among various methods and methods, while there are significant differences in the qualitative evaluation of samples using the methods and reagents used, and further improvement is needed.
Keywords: Different nucleic acid extraction methods; novel coronavirus Nucleic acid test; Interventricular quality assessment
新型冠状病毒( 2019 Novel Coronavirus, 2019-nCoV )是一种严重危害人类健康的传染病。国际病毒分类协会将其命名为严重急性呼吸综合征冠状病毒2(Severe Acute Respiratory Syndrome Coro-navirus 2, SARS-CoV-2)。在我国,将逆转录实时荧光定量聚合酶链式反应( Reverse Transcription Quantitative Real - time Poly-merase Chain Reaction, RT-qPCR )检测对新型冠状病毒的核酸进行快速、准确、准确的诊断和疗效监控。目前,大多数已经登记的新冠病毒核酸检测试剂都是将新冠病毒核酸检测试剂多以开放阅读框架lab(Open Reading Frame lab, ORFlab)基因、核衣壳蛋白(Nucleocapsid, N)基因和囊膜蛋白(En-velope, E)基因作为检测的目标,并将其与内源性内标物(IC)基因结合起来,来进行新型冠状病毒的核酸检测。有些医院可能会出现一些问题,比如:新冠核酸检测的结果会出现一些与患者的临床表现不符的现象,比如:假阴性较高;有很多因素会对新冠病毒核酸检测的效果产生影响,虽然大部分的实验室都在注重检测试剂的性能,但事实上,在RT-qPCR检测的过程中,核酸的纯度和浓度也会起到非常关键的作用。所以,根据当前所存在的问题,本研究通过选取的60例PCR实验室使用的两种不同的核酸提取技术及两种不同的2019- nCoV核酸试剂,对两种不同的2019- nCoV核酸进行了系统的对比,并对其进行了初步的分析。
1.资料与方法
1.1一般资料
样品:选取2019年至2020年检验中心发放的新冠病毒核酸检测的样本60例。
1.2方法
1.仪器及试剂:SLAN-96P (上海宏石)、广州达安基因股份有限公司、(新型冠状病毒(2019- nCoV)核酸检测试剂盒(批次:20200302)和磁珠法核酸提取试剂盒(批次:SDK60105)来自于上海思路迪生物医学科技有限公司,另一种新型冠状病毒(2019- nCoV)核酸释放剂(批次:2020076)来自于广州达安基因股份有限公司。
2.方法在接受实验室质量评定样品的当日,立即进行实验室质量评定。生物安全性保护按照《新型冠状病毒感染的肺炎实验室检测技术指南(第五版)》的规定执行;按其对核酸的提取及扩增作用,可将其分成3组。(1)磁珠法核酸提取试剂+核酸检测试剂+A(2)核酸释放剂+核酸检测试剂+B,(3)核酸磁珠提取试剂+ 核酸检测试剂+B[1]。
3.DNA提取(1)磁性微球:将 A公司的 DNA提取试剂与上海思路迪全自动核酸提取仪结合,对样品进行质量评定,使样品混合均匀后,抽取200微升,添加到对应的深孔板第-列中,置于提取仪中,按对应步骤进行自动化提取;(2)核酸释放剂方法:将10微升 B公司样品的核酸释放剂置于八联管内,经质量评定样品混合均匀后,取10微升至八联管内,混合均匀后放置10 min。一切都是根据试剂使用说明来操作的。
4.按照试剂说明,制定一个反应系统,设定一个反应步骤,用宏石SLAN-96P型自动荧光 PCR扩增仪和一种核酸扩增试剂,对其进行扩增试验,并对试验结果进行判断。A公司的 PCR反应系统为25微升,包含7.5微升的RT-PCR反应溶液、5微升的酶混合液、4微升的新冠三段反应溶液、脱氧核糖核酸酶H203.5微升和5微升的核酸模板样品。PCR反应条件为:50℃反转录,30分钟;5分钟的预退态95℃;在45个周期中,退火,延伸,荧光测定,共进行45次。结果解读:当 FAM (ORF1ab). ROX (N)和 HEX (内标物)3个信道 Ct≥35并且放大曲线呈 S型的时候,判断为该基因的检测是阳性的;如果 Ct>38,则为阳性;当35< Ct<38时,我们认为这是一个灰色区域,需要再次检查,如果两次检查都处于“灰区”相关研究已经发现了一个新的,将两次检查的平均数据,即报告的 Ct值。B公司为该核酸检测试剂制备了50微升的 PCR反应系统,包含26微升的RT-PCR反应溶液,4微升的酶类混合物,20微升的核酸模板样本;PCR反应条件:50℃反转录,30min;1分钟的预退变95℃;45次的退火,延伸和荧光测定,60℃30s,冷却时间25℃10s。结果解读:在 FAM (ORF1ab)、 ROX (N)、 HEX (内标)3个通道中, Ct≥40,并且扩增曲线呈 S型曲线的,可以判断为该基因的检测结果是阳性的,如果 Ct>40,则可以判断为该基因的检测结果是阴性的,如果出现了不正常的情况,则需要重新进行检查[2]。
5.质控用具应附有负、正对照品,当负、正对照品测试在受控状态时,此批测试的结果为正确的;如果负、正控制的测试结果没有得到控制,那么这一批测试的结果就是无效的。制作1份环境评价样品,作为阴性对照,将其置于 PCR试验的 I区域,以质量评价样品的检验方式进行检验,以确定是否存在环境污染。
1.3统计学方法
在这一次的观察和研究中,笔者使用了SPSS25.0作为数据统计分析工具,通过t检验对比的差异,以从数据层面获得有效的量化解释。
2.结果
2.1不同基因碱处理分析
磁珠法+A或者B公司的检出率更高,且P<0.05,见表一。
表一两组患者护理后心态评分比较
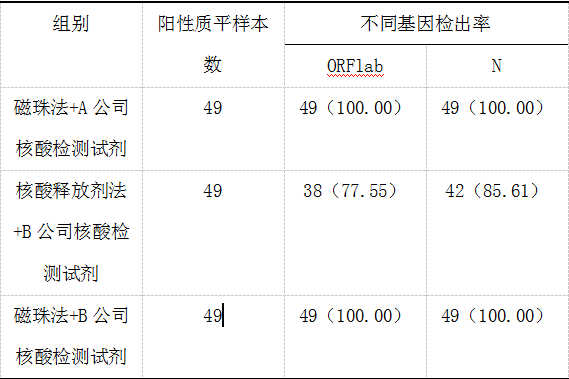
2.2两组患者双基因同时间处理及检出有效率比较
磁珠法+A或者B公司的检出率更高,且P<0.05,见表二。
表二 两组患者双基因同时间处理及检出有效率比较
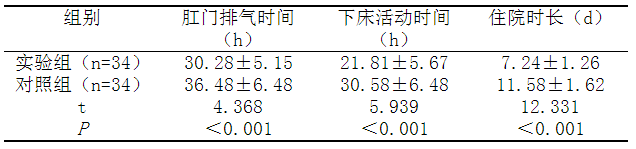
3.结论
2019- nCoV (2019- nCoV)感染的精确诊断是决定临床救治方案和控制感染的重要因素。本课题拟采用本院现有两种2019- nCoV核酸试剂和两种不同的提取方式,对两种不同的2019- nCoV核酸进行系统的分析。RT-qPCR以其高灵敏、高特异、操作简便、快速等优点,已成为目前最重要的新型冠状病毒核酸检测技术。然而,目前采用RT-qPCR检测新冠病毒存在着较高的假阴性率,检测结果与临床表现不符等问题。在影响核酸检测结果的诸多因素中,高纯度和高质量的核酸是一个重要的因素。本次选择的核酸提取试剂盒都是采用人工提取的方式,其中包含了磁珠法和 DNA提取法两种方法。由试验结果可知,使用 A、 B两家公司生产的磁性微球方法所得到的样品,其检出率均为100%。然而,采用 B公司的核酸释放剂法,其对ORF1ab和 N基因的检出水平分别为70%和90%,表明其对ORF1ab和 N基因的检出水平不高。但是,通过使用 B公司的核酸检测试剂,对质评样品进行了检测,得到的结果显示,所有阳性样品的 Ct值都比其它两种组合要小,这证明了该试剂组合对室间质评阳性样品都可以更敏感地检测出目标基因。
此次实验室内质量评价主要考察的是实验室样品的处理、提取和检验,不包括临床样品的收集、运输和报告的分发。2019- nCoV可通过肺部灌洗液、鼻腔痰液、排泄物及血液等进行核酸分析。对同一患者进行定量化验,若取样时间不当,则在不同病程和疾病的患者体内不同取样位置的病毒含量会有差异。另外2019- nCoV是一种 RNA病毒,很容易被分解,所以在收集到样品后必须严格按规定运输,这样才能最大程度的确保检测结果的精准程度,降低检测过程中出现的误差现象,为临床分析和判断提供精准的数据依据。
新冠肺炎作为一种紧急的公众健康问题,若不及时对其进行有效的控制,将会影响整个社会的安定以及人们的生命健康安全,因此,必须在最短的时间内对相关的人员进行检测,在确保检测结果精准度的情况下,有效的控制疫情的扩散和发展。各个试剂公司在很快的速度下,试剂箱的研制与批准都是在很快的时间里进行的,因此,在测试剂的品质以及一些性能指标上,不可避免地存在着一些瑕疵,这就给我们的实验室提出了更高的品质管控。各个实验室应结合自己的实际条件,尽量选用能够使检测结果有较大改善的检测结果,从而使检测结果更为准确,才能进一步确定病源,进而对控制疫情的扩散提供精准的依据。
在本次试验中,只对2种检测方式进行研究,使用的国家卫健委临检中心和本省临床检验中心的室间质量评价样品进行了一个比较分析,由于样本量比较小,因此不一定能够反映出2种检测方式的总体检测能力。在我国,由于疾病进展缓慢,实验材料匮乏的情况下,如果能够获得大量的阳性样品,就能够更好地评估各种药物的提取与放大效果。
参考文献:
[1]刘婷,欧阳政德,吴文金,等.两种不同释放剂核酸提取法的新型冠状病毒RT-PCR内标检测结果比较[J].中国热带医学,2021,21(2):5.
[2]黄裕游,何雪芳.4种不同核酸提取试剂在自建新型冠状病毒核酸检测系统中性能比较[J].检验医学与临床,2022(019-013).